|
Un aspecto crucial a todo el crecimiento normal de la célula lo constituye una red de comunicaciones que funcione apropiadamente. Esta red es una colección intrincada de mecanismos construidos con proteínas interactivas. Junto con estos mecanismos, el señalamiento preciso de proteína a proteína permite una regulación muy cuidadosamente protegida del crecimiento. Aquí se presentan algunos ejemplos de los mecanismos celulares.
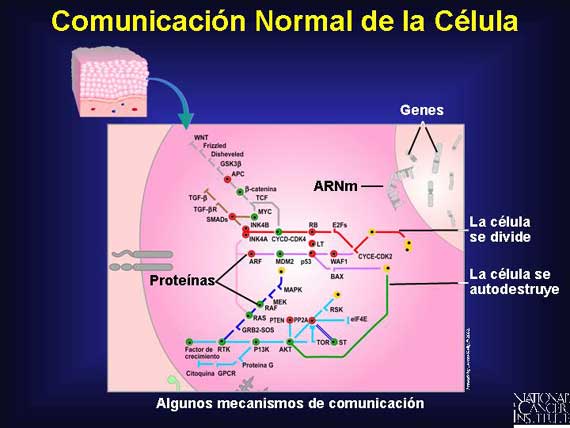
Los cambios genéticos involucrados en el cáncer resultan en proteínas alteradas que interrumpen la red de comunicación de la célula. En el cáncer, las proteínas alteradas a lo largo de muchos mecanismos diferentes causan que las señales sean confusas, interceptadas, amplificadas o dirigidas erradamente. Estos cambios secuestran lo que una vez era una comunicación normal y la utilizan para lograr alcanzar un crecimiento tumoral descontrolado. Aquí se presentan algunos ejemplos de la manera en que el cáncer interrumpe los mecanismos celulares normales.
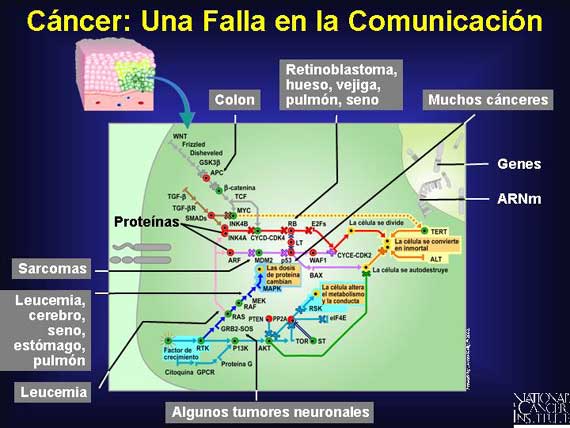
El reto para la detección y el diagnóstico del cáncer es localizar a los genes y a las proteínas renegadas-las moléculas trastornadas, defectuosas y dominantes-que secuestran la comunicación en células que fueron una vez normales. Esto requiere el abrir la célula y el analizar las biomoléculas dentro de ella. Entre más pronto pueda ocurrir esta detección y diagnóstico, es mejor.
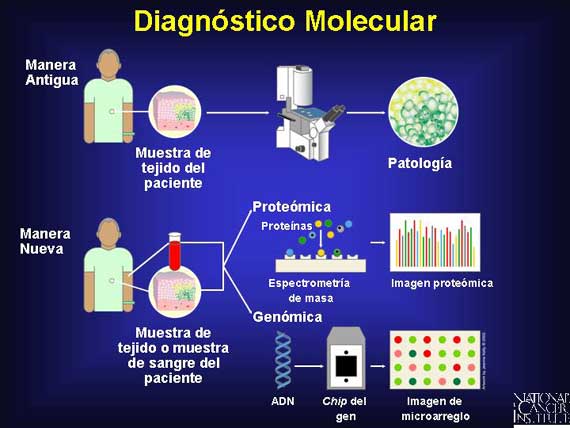
Antes de que existiera el diagnóstico molecular, los clínicos clasificaban a las
células cancerosas de acuerdo con su patología, es decir, de acuerdo con su
apariencia bajo el microscopio.
Pidiendo prestado de dos nuevas disciplinas, la genómica y la proteómica, el
diagnóstico molecular clasifica al cáncer utilizando tecnología como la
espectrometría de masa y los chips de genes. La genómica es el estudio de todos
los genes en una célula u organismo, mientras que la proteómica es el estudio
de todas las proteínas. El diagnóstico molecular determina la manera en que
estos genes y proteínas están interactuando en una célula. Se enfoca en
patrones-patrones de actividad de los genes y las proteínas-en diferentes tipos
de células cancerosas o precancerosas. El diagnóstico molecular descubre estos
conjuntos de cambios y captura esta información como patrones de expresión.
También conocidos como "firmas moleculares", estos patrones de expresión están
mejorando la habilidad de los clínicos para diagnosticar el cáncer. Pronto
todos los cánceres podrán ser diagnosticados de esta manera.
 |
Un mayor énfasis en el diagnóstico molecular es puesto en los patrones de
expresión de genes. El reto es encontrar a los genes activos en el cáncer y
separarlos de todos los otros en una célula. Afortunadamente, la nueva
tecnología hace que el éxito sea posible. Los microarreglos (micromatrices) de
ADN, algunas veces conocidos como "chips de genes", le permiten a los
investigadores "observar" la expresión de cientos o miles de genes todos al
mismo tiempo.
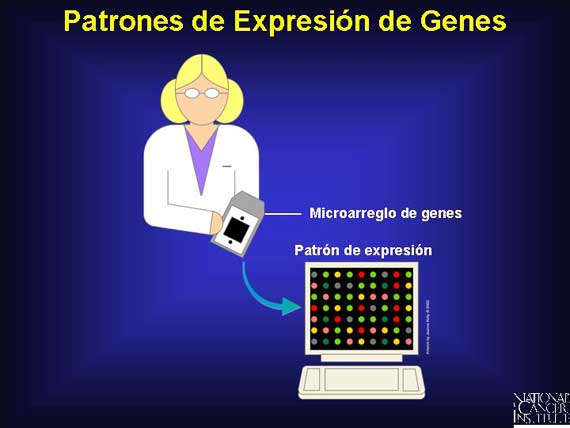
Para apreciar la manera en que el diagnóstico molecular utiliza los microarreglos de ADN para medir la actividad de genes, usted primero debe entender un poco acerca del genoma humano, acerca del ADN genómico y del enlace del ARN mensajero a su expresión. Usted también debe recordar que los patrones de expresión de genes variarán con el tipo de célula por todo el cuerpo humano.

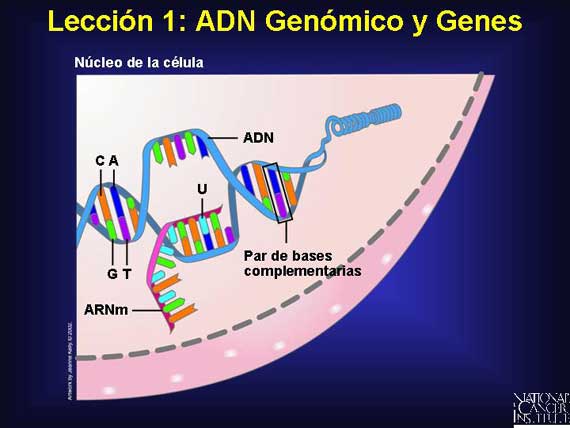
El genoma humano es el juego completo de "instrucciones" genéticas para la vida humana. Esta información reside en los genes dentro de moléculas muy grandes del ácido desoxirribonucléico (ADN). El ADN en el genoma humano que es transferido a la progenie como información necesaria para la supervivencia se conoce como ADN genómico.
Las moléculas grandes de ADN están compuestas de dos cadenas enrolladas alrededor la una de la otra para formar una "doble hélice". Cada cadena está constituida de millones de bloques químicos de construcción conocidos como "bases". El ADN contiene sólo cuatro bases diferentes (abreviadas A, T, G, C), pero ellas se pueden arreglar en cualquier secuencia. El orden de las bases determina el mensaje que el gen contiene, de manera similar a como las letras del alfabeto se pueden recombinar para formar nuevas palabras. Las secuencias de bases de las dos cadenas de cada molécula de ADN están relacionadas cada una con la otra por la siguiente regla: A sólo se corresponde con T, y C sólo se corresponde con G. Por lo tanto, la secuencia de bases en una cadena dicta el orden de las bases en la otra cadena. Esto se conoce como "apareamiento de bases" y le permite al genoma copiarse a sí mismo y transferir el ADN genómico a la siguiente generación.
 |
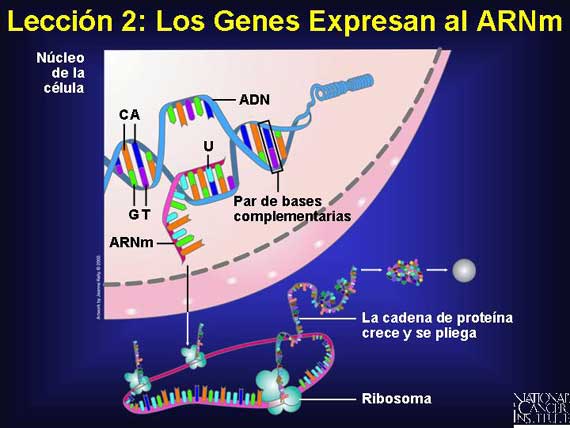
Cuando un gen se expresa a sí mismo, se "activa" para producir una proteína. El gen lo hace así, primero dirigiendo la síntesis de una molécula intermediaria conocida como ácido ribonucléico mensajero (ARNm). Para transferir la información de un gen del ADN al ARNm, se utiliza el apareamiento de bases. Sin embargo hay un cambio. El ARN utiliza una nueva regla: A se corresponde únicamente con U y C se corresponde únicamente con G. Por lo que la secuencia de bases de una molécula de ARNm se parece a aquélla de la molécula del ADN de la cual fue copiada, excepto que la base U aparece en todas las partes en donde la base T aparecería en el ADN.
 |
Diferentes tipos de células expresan un conjunto distinto de ARNms de sus genomas. Por ejemplo, aunque tanto una célula muscular (miocito) como una célula inmune (linfocito) poseen el mismo ADN genómico heredado, las redes reguladoras dentro de cada tipo de célula causan diferentes subconjuntos de estos genes para ser expresados como ARNm. Y algunas veces diferentes tipos de células expresan los mismos ARNms, pero un tipo de célula producirá más copias que la otra.
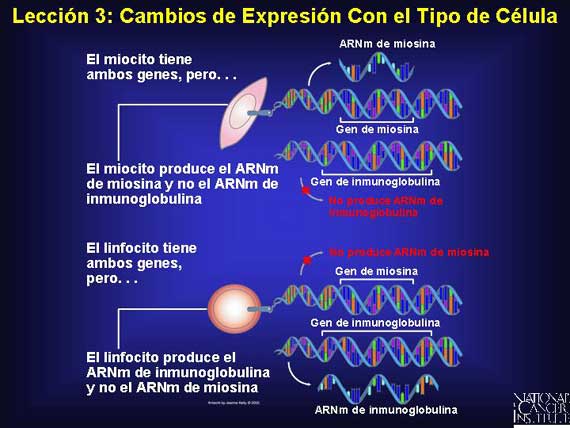
En cualquier momento dado en cada célula del cuerpo, miles de genes diferentes están activos. Hasta hace poco no había sido posible capturar y comparar los patrones de expresión de genes presentes en diferentes células de alguna manera sistemática. Los microarreglos de ADN permiten la comparación de miles de genes que pueden ser medidos simultáneamente y la información ganada utilizando estos arreglos está cambiando dramáticamente las decisiones sobre el tratamiento del cáncer.
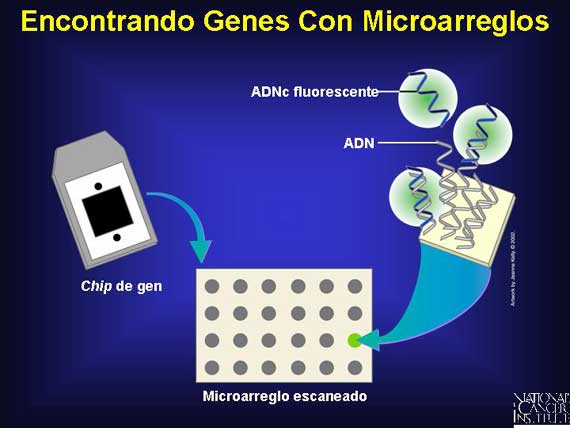
Un microarreglo de ADN es un chip de tamaño muy delgado que ha sido detectado en
localizaciones fijas con miles de fragmentos de ADN de cadena individual que
corresponden a los diversos genes de interés. Un microarreglo individual puede
contener 10,000 ó más sitios, cada uno de ellos conteniendo piezas de ADN de un
gen diferente. Un chip de gen individual puede hasta contener fragmentos
representativos del genoma humano completo.
 |
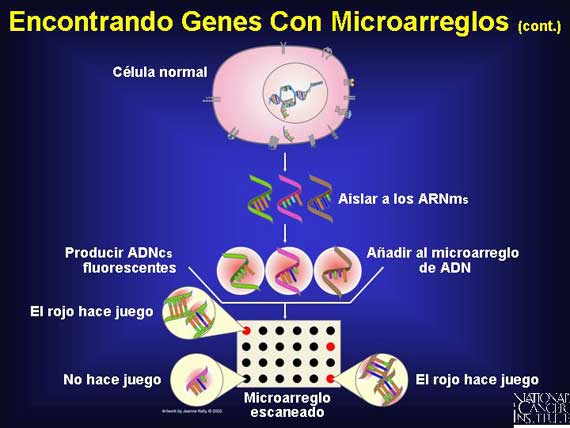
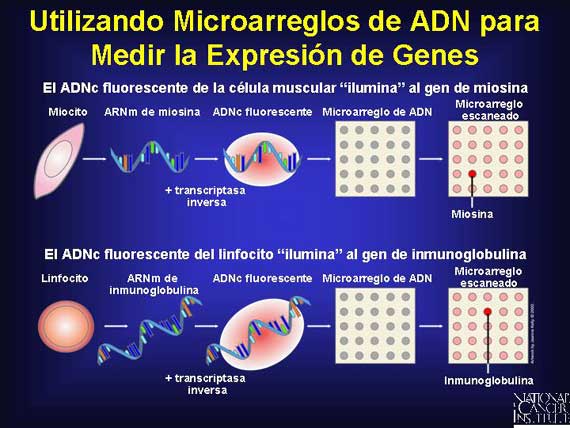
Para determinar cuales genes están siendo expresados en una población celular determinada, las moléculas del ARNm, las cuales son producidas por genes activos a medida que ellos ensamblan proteínas, son aisladas de las células y copiadas con una enzima especial conocida como "transcriptasa inversa". La enzima copia la cadena de ARNm utilizando la regla del ADN (consulte la transparencia 8) y la copia se conoce como un ADNc. Por lo tanto, cada ADNc producido utilizando la transcriptasa inversa corresponde directamente a un ARNm específico que provino de un gen activo en la célula.
Todos los ADNcs son entonces unidos a un colorante fluorescente. Cuando el microarreglo de ADN es bañado con los ADNcs fluorescentes, cada molécula de ADNc se unirá por apareamiento de bases al sitio en donde las piezas de su gen correspondiente específico están localizadas. Por lo tanto, cada sitio fluorescente en el microarreglo corresponde a un gen que fue activamente transcrito dentro del ARNm en la célula original.
 |
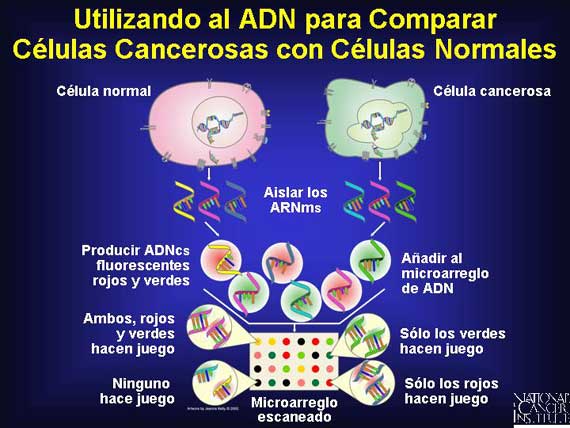
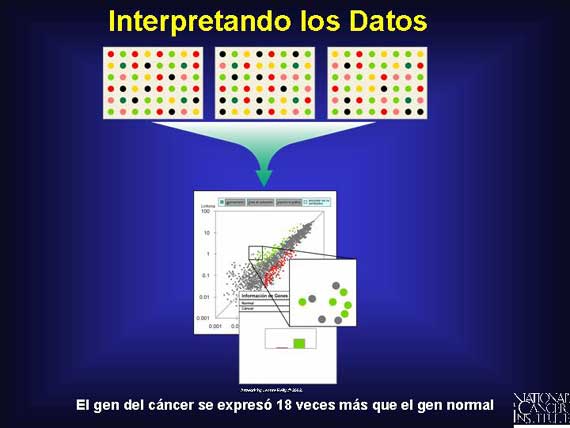
Además de ser utilizados para evaluar la actividad de los genes que se están expresando en una muestra individual, los microarreglos de ADN también se pueden utilizar para comparar los patrones de expresión de genes en dos poblaciones de células diferentes, como por ejemplo, una población de células cancerosas con una población de células normales. En este caso, se utilizan dos colorantes fluorescentes diferentes. Por ejemplo, un colorante rojo puede identificar a los ADNcs derivados de las células normales correspondientes y un colorante verde puede identificar a aquéllos derivados de las células cancerosas. Cuando los ADNcs rojos y verdes se combinan y se colocan en un microarreglo de ADN, los ADNcs verdes se unirán a los genes expresados en las células cancerosas y los ADNcs rojos se unirán a los genes expresados en las células normales. Los sitios verdes representan más copias de un gen que se están produciendo en una célula cancerosa y los puntos rojos significan que más copias se están produciendo en la célula normal. Los puntos amarillos, causados por la mezcla de fluorescencia roja y verde, representan los genes cuya expresión es aproximadamente la misma en ambos tipos de células, y los puntos negros, o la ausencia de fluorescencia, representan los genes expresados en ninguno de los dos tipos de célula.
 |
Los microarreglos hacen posible comparar la expresión relativa de miles de genes en las células cancerosas y normales midiendo la intensidad y el color de la fluorescencia de cada sitio. Un programa de computadora (ordenador) puede entonces analizar los datos y hacer mediciones precisas de los genes expresados a niveles altos y a niveles bajos. La mayoría de los estudios de microarreglos ahora incluyen "análisis en racimo", el cual agrupa a los genes que tienen niveles similares de expresión.
 |
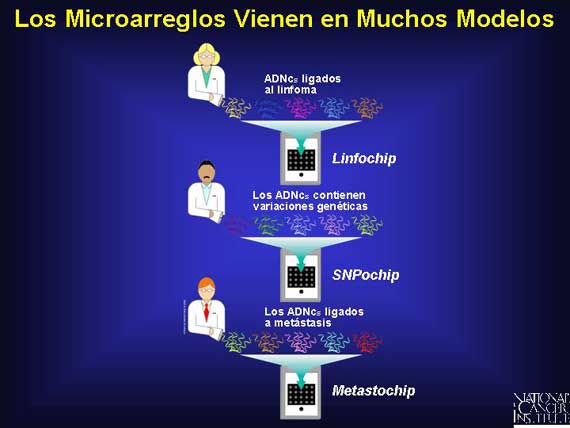
Hay algunos microarreglos estándares para su uso en la investigación del cáncer,
como por ejemplo, el Linfochip (Lymphochip, en inglés). Los arreglos estándares
incluyen a genes que han sido reportados como importantes en un cierto tipo de
cáncer. Otros arreglos contienen cadenas de ADN conocidas como polimorfismos de
nucleótido único (single nucleotide polymorphisms, SNPs o "snips", en inglés),
los cuales son variaciones comunes en el ADN. Los investigadores también pueden
crear sus propios microarreglos utilizando cualquier gen (o fragmentos de gen)
que ellos piensen que podría ser importante a las preguntas que ellos están
tratando de contestar.
 |
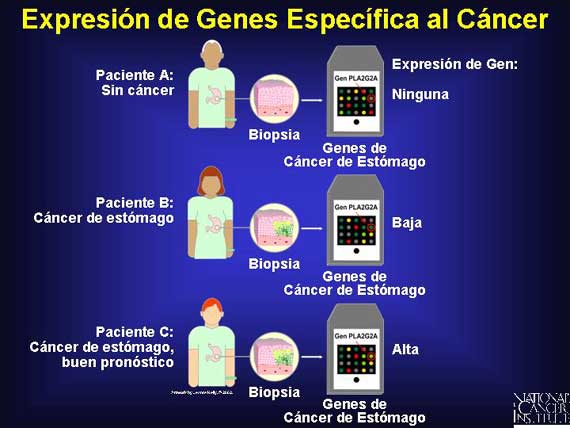
Los microarreglos se están utilizando en la investigación del cáncer con
resultados increíbles. Por ejemplo, los investigadores utilizaron microarreglos
para comparar los patrones de actividad de genes en tejido de estómago normal y
tejido de tumores del estómago. Ellos encontraron que el tejido del tumor, pero
no el tejido normal, expresó un gen conocido como PLA2G2A. Pero ellos también
encontraron que los pacientes con cáncer con niveles de expresión altos del gen
PLA2G2A tuvieron una probabilidad mayor de sobrevivir por 5 años, comparado con
los pacientes cuyos tumores produjeron niveles más bajos.
 |
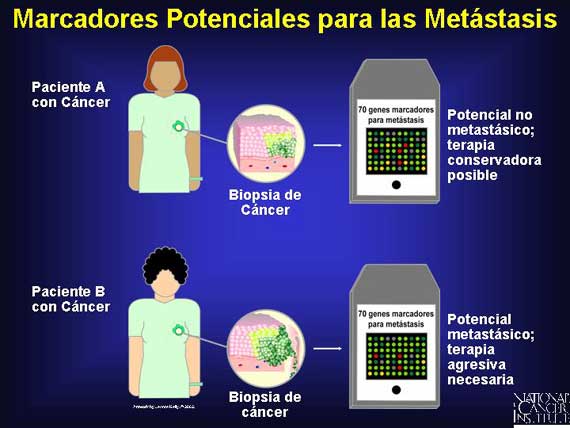
Los patrones de expresión de genes también se están utilizando como una herramienta para mejorar el diagnóstico de cáncer de seno. Los microarreglos han sido utilizados para examinar los patrones de expresón de unos 25,000 genes en tejidos de pacientes con cáncer de seno. El análisis en racimo por medio de computadora (ordenador) de los patrones condujo a la identificación de casi 70 genes marcadores que pueden identificar correctamente alrededor de un 90 por ciento de las mujeres que eventualmente desarrollarán metástasis. Aunque son aún experimentales, dichos estudios brindan esperanza de que los clínicos podrán actuar mucho más pronto y utilizar nueva tecnología para monitorear mejor a las mujeres con una probabilidad mayor de experimentar progresión agresiva de sus cánceres de seno.
 |
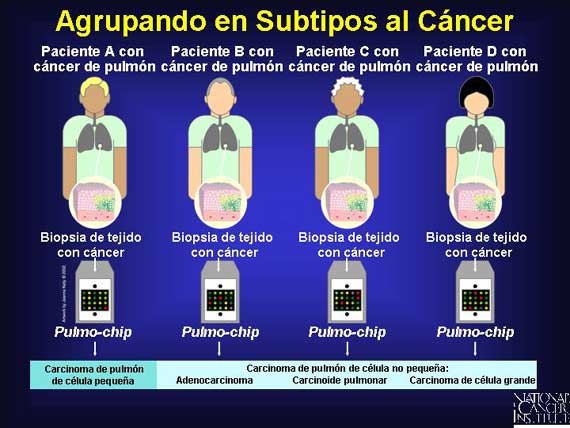
Los investigadores también utilizan microarreglos para detectar las diferencias en los patrones de actividad genética aún en el mismo tipo de tumor. En muchos casos, los investigadores han descubierto que lo que había sido considerado un tipo individual de cáncer-basado en la manera en que las células se observaban bajo el microscopio-era en realidad dos, tres o aún más subtipos, cada uno con un patrón de expresión de genes distinto. Por ejemplo, utilizando los microarreglos, los investigadores han identificado nuevos tipos de leucemia y descubierto que el tipo de cáncer de pulmón más común (adenocarcinoma de pulmón) es en realidad cuatro tipos distintos de cánceres, cada uno con su propio patrón de expresión de genes.
 |
Uno de los primeros descubrimientos de los subtipos de cáncer ocurrió en un
cáncer de la sangre conocido como linfoma de célula B grande difusa (el subtipo
más común de linfoma no de Hodgkin). Utilizando un chip que contenía fragmentos
de 18,000 genes, los investigadores encontraron dos subtipos de cáncer
distintos. Estos cánceres se veían iguales bajo el microscopio, pero tenían
patrones diferentes de actividad genética.
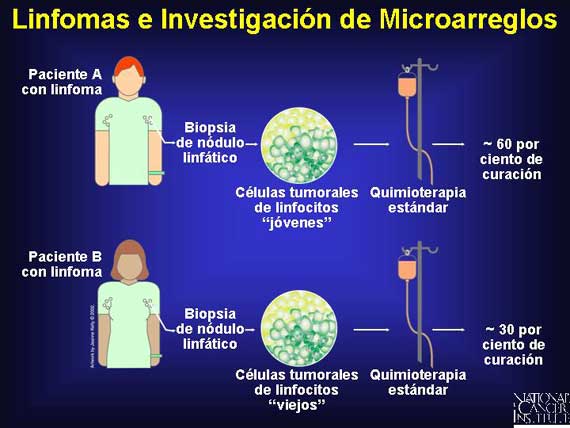
Los subtipos también eran diferentes en otras maneras. Para empezar, ellos se
originaron de diferentes tipos de células. Las células tumorales de un subtipo
de cáncer se originaron de linfocitos menos diferenciados ("jóvenes"), mientras
que el otro subtipo se originó de linfocitos más diferenciados ("viejos").
También hubo una diferencia en la supervivencia entre los dos tipos. Alrededor
de un 60 por ciento de las personas con el subtipo "joven" respondieron a la
quimioterapia, comparado con sólo un 30 por ciento de las personas con el
subtipo "viejo".
 |
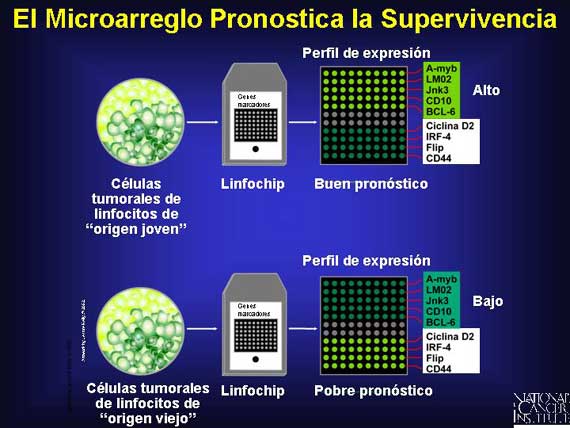
Dos años después, otro análisis de chip de gen reveló un tercer subtipo de linfoma de célula B grande difusa. También produjo otro avance: Los investigadores encontraron 17 genes que estaban fuertemente relacionados con la supervivencia. Los científicos crearon una fórmula para pronosticar la respuesta a la quimioterapia en base a los patrones de expresión de estos 17 genes. Esta fórmula dividió a los pacientes con linfoma de célula B en cuatro grupos. Dos de los grupos tuvieron tasas de supervivencia de alrededor de un 72 por ciento 5 años después del diagnóstico. El tercer grupo tuvo una tasa de supervivencia de 34 por ciento y el cuarto grupo tuvo una tasa de supervivencia de 15 por ciento. La fórmula pronosticadora de los 17 genes fue mejor que cualquier otro método actual en la identificación de pacientes con el peor pronóstico. Una identificación como esta es importante ya que si los pacientes a los que se les pronostique pobres resultados pueden ser identificados correctamente en una etapa temprana de tratamiento, ellos pueden recibir terapias más agresivas inmediatamente en lugar de tener que esperar hasta que las terapias estándares fallen.
 |
Otro uso importante de los microarreglos ocurre en la farmacogenómica, un área de la investigación que estudia el por qué ciertos medicamentos funcionan en combinación con patrones de expresión genética en particular pero no con otros. Esta información está siendo utilizada para diseñar nuevos medicamentos que ponen como objetivo a las células cancerosas sin afectar a las células normales.
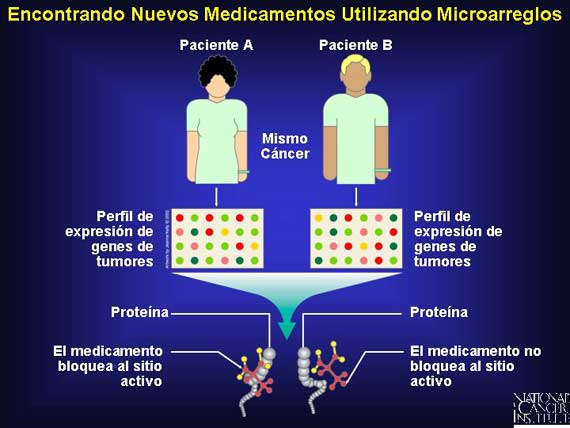
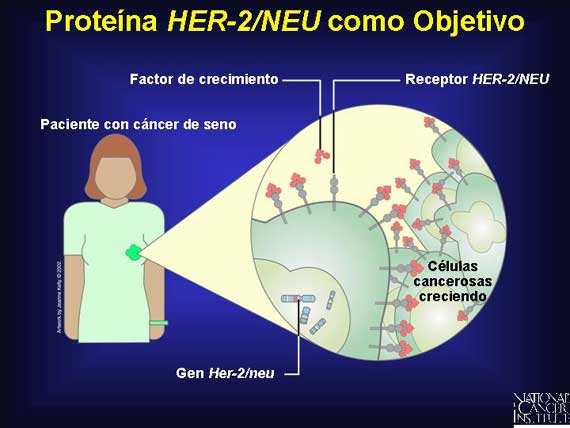
La Herceptina es un buen ejemplo de una historia con éxito de la
farmacogenómica. En los '80s, los investigadores descubrieron que algunas
mujeres que tenían cánceres de seno de crecimiento particularmente rápido
expresaron copias adicionales de un gen conocido como Her-2/neu. Los genes
estaban produciendo muchas copias de una proteína que parecía estar activando
el crecimiento de las células cancerosas.
 |
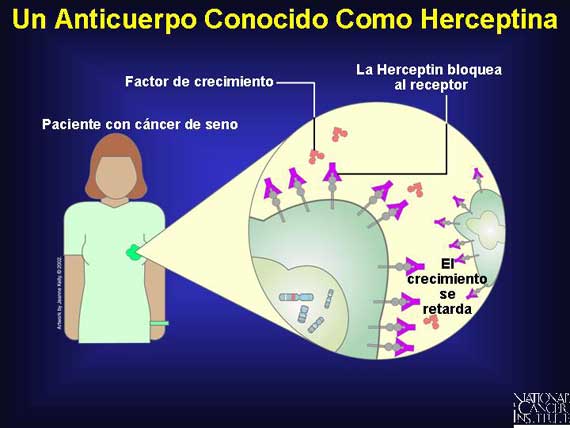
A principios de los '90s, se desarrolló un anticuerpo que se une a las proteínas
her-2/neu en la superficie de una célula cancerosa. Evita que las proteínas
proporcionen incentivos para el crecimiento de células cancerosas y a través de
esta "señal de detención" también pueden detener la propagación de las señales
de supervivencia dentro de la célula cancerosa. Algunas mujeres a las que se
les proporcionó el anticuerpo experimental observaron que su crecimiento
canceroso se retardó o se detuvo por completo cuando su tratamiento con
Herceptina fue combinado con la quimioterapia citotóxica.
La Herceptina fue aprobada por la Administración de Alimentos y Fármacos (Food
and Drug Administration) a finales de 1998 como tratamiento para las mujeres
que tienen pruebas positivas para niveles altos de la proteína her-2/neu
(alrededor de un 25 a un 30 por ciento de todas las pacientes con cáncer de
seno).
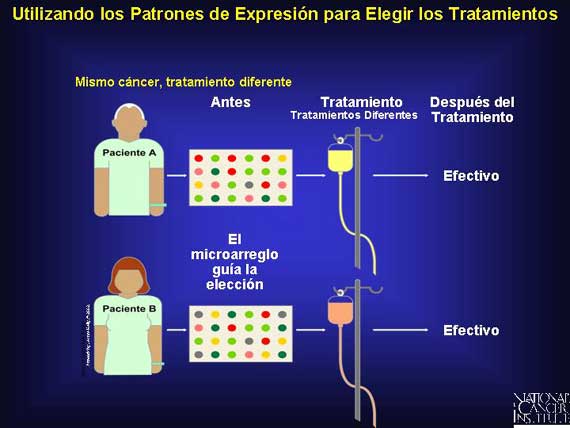
Con la llegada de los microarreglos, la investigación farmacogenómica ha entrado en un nuevo y completo nivel de sofisticación. Esta tecnología le permite a los investigadores estudiar a poblaciones de pacientes y recolectar patrones de expresión de tumores antes de que se proporcione cualquier tratamiento.
Al analizar los resultados del tratamiento, los científicos esperan identificar patrones de expresión que puedan pronosticar con precisión una buena respuesta al tratamiento. En el futuro, antes de que se administre algún tratamiento, los médicos tal vez podrán pronosticar la respuesta de un paciente a la quimioterapia o radiación en base a esta investigación. Esto podría eliminar mucho de la "adivinanza" clínica. Algún día, simplemente al observar los patrones de expresión encontrados en una muestra individual de sangre o una biopsia pequeña de tejido, los médicos tal vez podrán decirle a un paciente cuáles de los medicamentos o tratamientos de radiación disponibles funcionarán mejor y cuáles no. Los clínicos podrán planear mejor terapias efectivas en las dosis apropiadas para los cánceres individuales.
 |
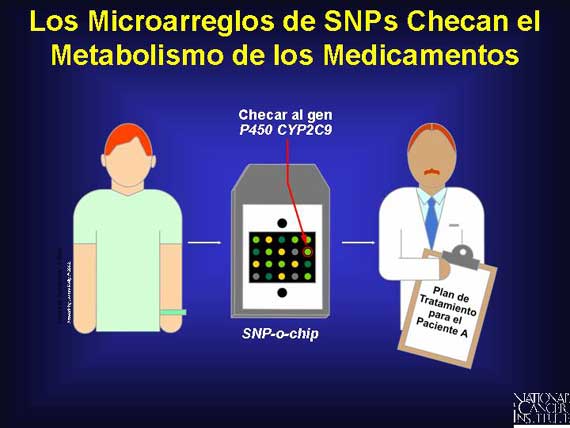
Los microarreglos también serán útiles en el estudio del metabolismo de
medicamentos. Los medicamentos son degradados en el cuerpo por proteínas y no
todas estas proteínas son idénticas de persona a persona. Las variaciones
genéticas conocidas como polimorfismos de nucleótido único (single nucleotide
polymorphisms o SNPs), pueden resultar en pequeñas diferencias en las proteínas
lo cual se traduce en diferencias mayores acerca de cómo funciona la proteína.
Por ejemplo, tanto como un 40 por ciento de las personas tienen un SNP que
causa una deficiencia en una proteína conocida como citocromo P450 CYP2C9, el
cual es importante para el metabolismo de los medicamentos. Las deficiencias en
esta proteína pueden dañar el metabolismo de 1 de cada 5 medicamentos que se
encuentran actualmente en el mercado.
 |
Otro enfoque principal del diagnóstico molecular observa más allá de los genes, hacia una investigación del proteoma. El término "proteoma" se refiera a todas las proteínas producidas por una célula, y el estudio de estas proteínas es la proteómica. La proteómica del cáncer está permitiendo el mapeo de los patrones de proteínas involucrados cuando los mecanismos celulares normales son secuestrados en apoyo del crecimiento maligno. En el tejido canceroso, algunas de las proteínas críticas para la comunicación normal están dañadas, inactivas, hiperactivas o perdidas por completo. El juego completo de proteínas desordenadas y dominantes trabajando para interrumpir las comunicaciones celulares puede variar de un tipo de cáncer a otro. Ellas también pueden variar algo de un paciente a otro dentro de un mismo tipo de cáncer.
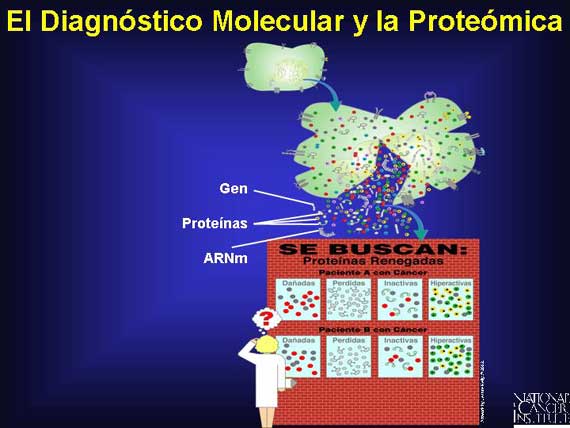
 |
Los investigadores del cáncer están concibiendo maneras inteligentes para capturar los datos sobre cada uno de los juegos de proteínas característicamente indóciles del cáncer. La biopsia o las muestras de sangre de pacientes con cáncer son el punto de inicio. Muchos métodos diferentes están siendo utilizados para extraer y analizar los diversos juegos de proteínas interactivas.
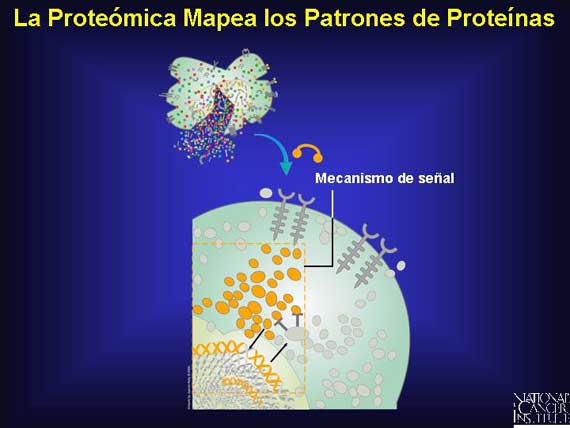
 |
Para muchas proteínas contenidas en la célula, la adición de una molécula pequeña llamada fosfato actúa como un interruptor que activa a la proteína. Este proceso se conoce como fosforilación. Para preservar el estado de fosforilación de una célula y capturar un patrón de proteínas preciso interactuando en una célula cancerosa, los investigadores proteómicos deben manejar los especímenes de la biopsia o de la sangre cuidadosamente. Ellos logran esto haciendo que las muestras sean rápidamente tratadas con enzimas para bloquear la remoción de los fosfatos de las proteínas. Esto le permite a los investigadores identificar un patrón de proteínas casi idéntico al que estaba contenido en la célula al momento de la recolección.
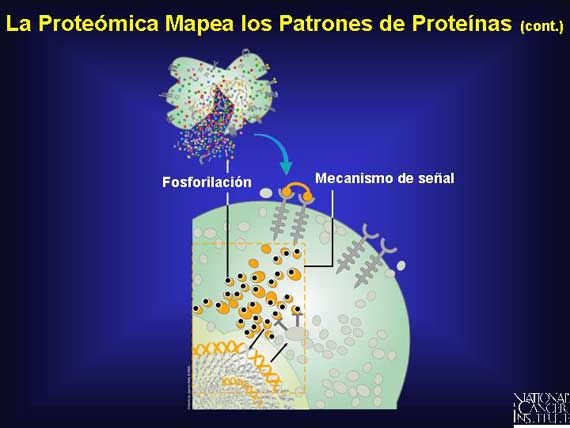
 |
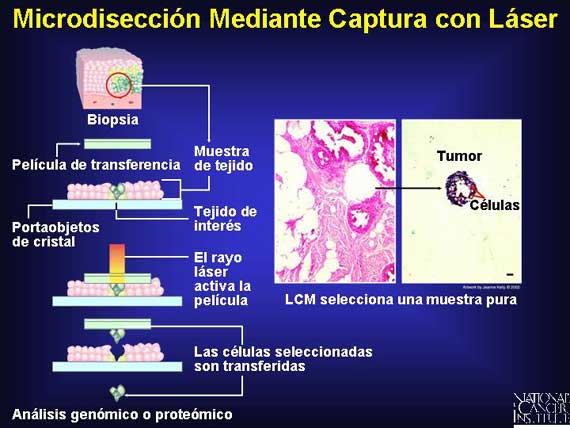
Un método que se está utilizando para minimizar el daño celular y capturar los
patrones de proteínas precisos en las células cancerosas y normales es la
microdisección mediante captura con láser (LCM, por sus iniciales en inglés).
Los investigadores utilizan un haz de láser de baja energía y una película
especial de transferencia para llevar una célula deseada fuera de la sección de
tejido, dejando todas las células no deseadas. Ellos pueden entonces recolectar
todas las proteínas que estaban presentes en las células seleccionadas, mapear
el patrón de proteínas y almacenar la información en una base de datos de
computadora (ordenador).
La microdisección mediante captura con láser ofrece varias ventajas para el
estudio de proteínas. Por ejemplo, con esta técnica los investigadores pueden
capturar juegos de células por separado de tejido normal, precanceroso,
canceroso y hasta tejido estromal, todos ellos de la muestra de biopsia del
mismo paciente.
Después de la microdisección mediante captura con láser, los científicos pueden extraer las proteínas y utilizar geles de dos dimensiones (2-D), microarreglos de lisado de proteínas y/o espectrometría de masa para separar e identificar subconjuntos de proteínas que pueden entonces servir como marcadores únicos en su género para un tipo de célula cancerosa en particular.
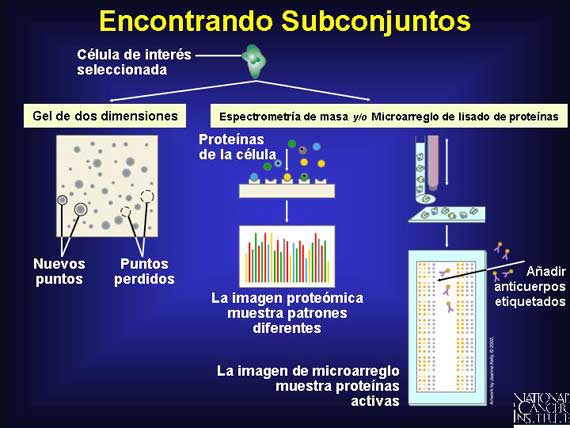
Los científicos han aprendido que no es necesario identificar a cada proteína
activa en el cáncer y capturada por la microdisección con láser. Para lograr un
diagnóstico molecular, lo único que puede ser necesario es separar y preservar
un subconjunto único, un patrón de proteínas compartido por todos los pacientes
con el mismo tipo de cáncer.
Por ejemplo, los investigadores recolectaron muestras de sangre de un grupo de
pacientes con cáncer de ovario diagnosticado. Ellos utilizaron espectrometría
de masa para recolectar todos los perfiles de proteínas que aparecieron en las
muestras de suero de las pacientes. Aunque hubo alguna variación de paciente a
paciente, el agrupar suficientes muestras de cáncer de ovario confirmado le
permitió a los clínicos utilizar análisis en racimo para determinar cual
subconjunto de proteínas consistentemente sirvió como marcadores para la
presencia del cáncer. La identificación de este subconjunto tuvo éxito y hoy en
día estamos en buen camino para completar un método de diagnóstico molecular
para el cáncer de ovario.
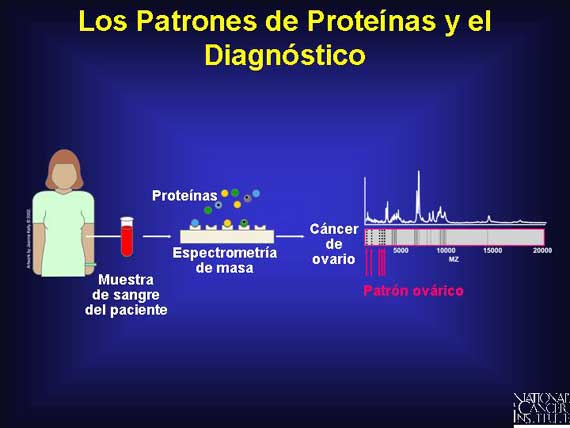
El diagnóstico molecular para el cáncer de ovario debe detectar correctamente a todas las mujeres que presentan este cáncer sin identificar incorrectamente a mujeres que no tienen la enfermedad.
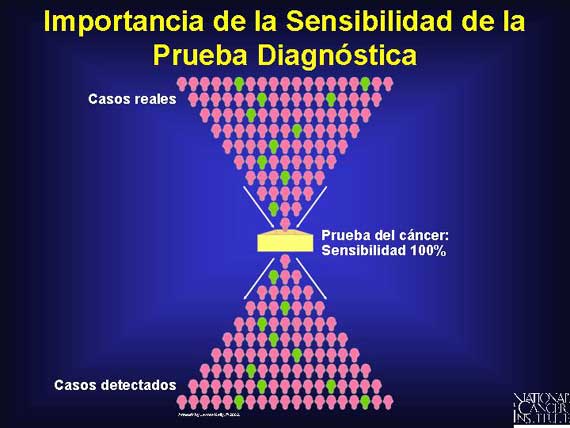
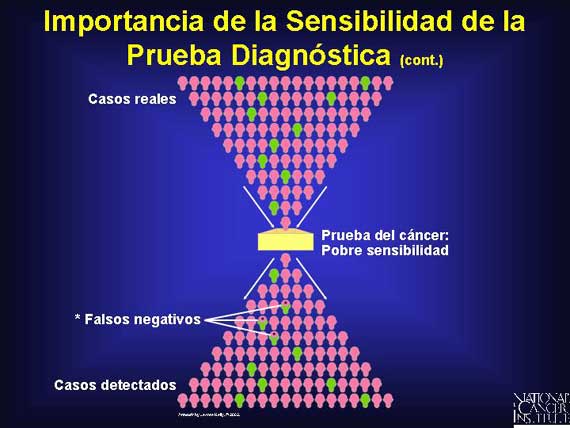
El primer obstáculo es la sensibilidad de una prueba. La sensibilidad contesta esta pregunta: ¿A qué porcentaje de personas con un tipo determinado de cáncer se les detectará su cáncer cuando se utilice una prueba de detección determinada? Si una prueba no es muy sensible, habrá muchos resultados "falsos negativos" y personas con cáncer no serán detectadas. Una prueba que produce muchos falsos negativos obviamente no será muy buena para reducir las muertes debidas al cáncer, dando un sentido falso de seguridad a personas que en realidad tienen la enfermedad.
 |
El siguiente obstáculo es la especificidad de una prueba. La especificidad contesta esta pregunta: ¿Qué porcentaje de las personas que no tienen cáncer son identificados correctamente de estar libre de la enfermedad? Si una prueba del cáncer no es muy específica, producirá muchos resultados "falsos positivos"; es decir, el resultado de la prueba de una persona será positivo aún y cuando ellos están libres de cáncer. Dicho error puede conducir a procedimientos de seguimiento innecesarios y costosos y causar ansiedad en la persona diagnosticada incorrectamente.

La alta especificidad es importante para una prueba de cáncer de ovario ya que este cáncer es una enfermedad relativamente rara, que ocurre sólo en alrededor de 1 de 2500 mujeres postmenopáusicas.
La prueba de diagnóstico de cáncer de ovario está siendo desarrollada y probada entre mujeres en riesgo de recurrencia de cáncer de ovario. Si este uso tiene éxito, la prueba luego será extendida a mujeres en alto riesgo de desarrollar la enfermedad.

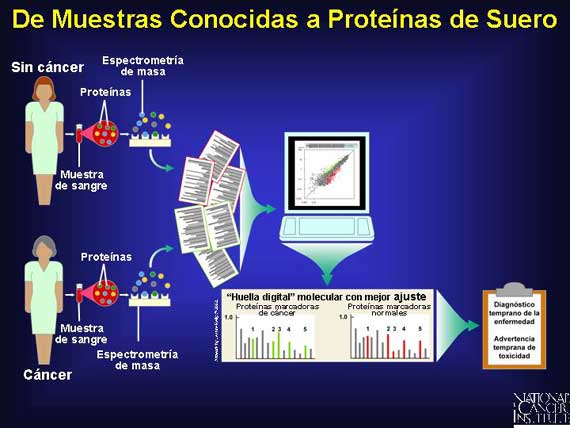
Los investigadores utilizaron los patrones de proteínas que ellos habían recolectado de las pacientes con cáncer de ovario junto con un programa de computadora (ordenador) de inteligencia artificial para crear y entrenar a una nueva herramienta de detección basada en la bioinformática. El programa fue diseñado para reconocer la presencia o ausencia de cáncer de ovario en muestras de sangre cuyo estado de cáncer se desconocía.

 |
Los científicos a continuación se preguntaron si una nueva herramienta de detección basada en la bioinformática para el cáncer de ovario podría ser creada utilizando proteínas de peso molecular bajo en los sueros de la sangre como biomarcadores. ¿Podría esta herramienta manejar con precisión los especímenes cuyo estado de cáncer es desconocido? Si es así, los investigadores podrían concebir una prueba mínimamente invasiva para la detección del cáncer de ovario en una etapa temprana. Si es así, su tecnología basada en la bioinformática podría tener también una aplicación amplia para el diagnóstico en una etapa temprana de muchos otros cánceres.
 |
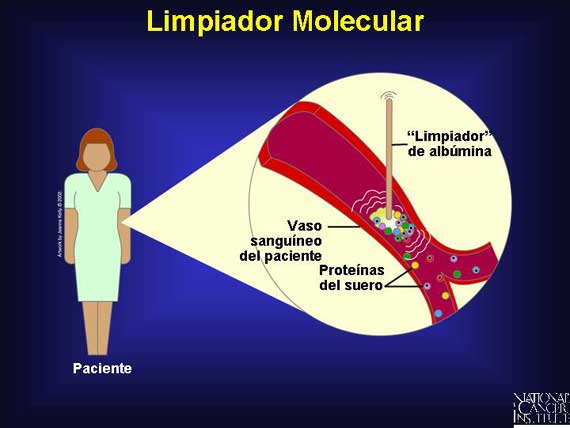
Un problema mayor en la identificación de los biomarcadores de cánceres son las muy bajas concentraciones de marcadores que provienen de tejidos con lesiones de cáncer pequeñas, en etapa temprana. Afortunadamente, los investigadores han encontrado una nueva manera de amplificar y concentrar estos biomarcadores en la sangre. Cuando los científicos buscaron patrones de proteínas en el suero de las pacientes con cáncer de ovario, ellos hicieron un descubrimiento interesante. La molécula de albúmina y otras proteínas portadoras de larga vida que circulan en el torrente sanguíneo actúan como limpiadores moleculares, atrapando una gran cantidad de proteínas de peso molecular bajo a medida que ellas se degradan y se preparan para la eliminación de la sangre. El "limpiador" en realidad les ayudó a recolectar y a amplificar, más de 100 veces, los patrones de proteínas de suero de baja abundancia necesarios para el análisis.
 |
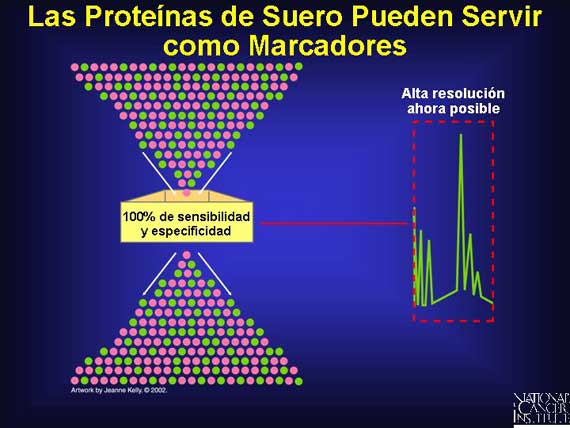
Los investigadores tuvieron éxito demostrando que un subconjunto de proteínas de peso molecular bajo del suero de pacientes formaron patrones predictivos que podrían ser utilizados experimentalmente para marcar la presencia de cáncer de ovario.
Ellos detectaron un patrón de diagnóstico de cinco proteínas en la sangre de mujeres con cáncer de ovario que no se encuentra en la sangre de otras mujeres. En un subconjunto limitado de pacientes de prueba, experimentalmente, la prueba ha tenido una sensibilidad de un 100 por ciento y una especificidad de un 100 por ciento.
Los clínicos han descubierto que el diagnóstico molecular tiene muchos usos más allá de la creación de nuevas herramientas de detección y diagnóstico. Los patrones de expresión también pueden proporcionar información para el diseño de nuevos tratamientos para el cáncer, para monitorear la eficacia del tratamiento a medida que se estudia en un estudio clínico, y hasta para predecir la respuesta del paciente a un nuevo tratamiento.

 |
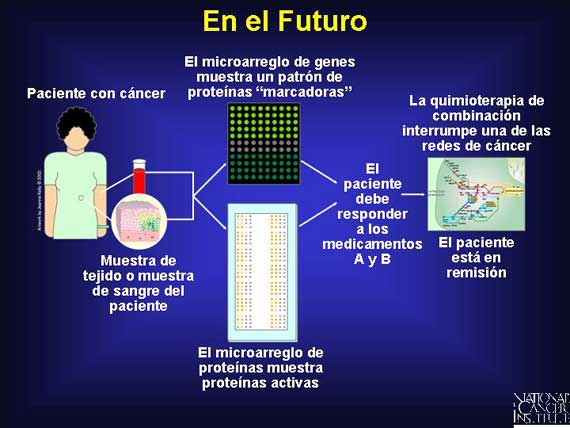
Imagínese lo siguiente: Una paciente con cáncer visita a su oncólogo, proporciona unas cuantas gotas de sangre o un espécimen de biopsia, y le dicen que su patrón de expresión genética muestra que ella tiene un cierto subtipo de la enfermedad. Mientras tanto, otro patrón de expresión pronostica que su perfil genético debe responder bien a los regímenes de quimioterapia A y B (con efectos secundarios mínimos). Durante sus tratamientos, los patrones de expresión de proteínas se utilizan para asegurarse de que su tratamiento esté efectivamente interrumpiendo el mecanismo celular objetivo en su tumor. Después del tratamiento, los patrones adicionales de expresión de genes y proteínas verifican que el cáncer está en remisión.
 |
El diagnóstico molecular y sus técnicas recientemente desarrolladas para examinar las firmas moleculares de células cancerosas-patrones de proteínas así como de genes-ofrecen una magnífica promesa para revolucionar nuestros enfoques de detección, al diagnóstico y a la clasificación de muchos diferentes tipos de cáncer. La participación en los estudios clínicos que validarán estos nuevos enfoques conducirá a mejoras significativas en el cuidado y atención de los pacientes con cáncer en un futuro no muy lejano.

|